感染已经是当前世界急危重症患者死亡的主要原因之一。据WHO统计,2019年,全球十大健康威胁,6个是感染性疾病!全球感染性疾病导致患者死亡占全部死因的25%以上,每年约1300万儿童死于感染性疾病。在中国,感染性疾病占所有疾病的50%以上,75%造血系统肿瘤患者和50%实体肿瘤患者死于感染,脓毒症(严重感染)患者病例率高达50%。
重症感染起病急、进展快、病原体复杂,基于高通量基因测序技术的宏基因组新一代测序技术(Metagenomic next-generation sequencing,mNGS)不依赖于培养,直接对临床样本中靶标核酸进行无偏倚、广谱性测序筛查,经严格校验与组织的微生物基因组数据库进行比对分析,能特异性鉴定人体微生物组种属,快速发现病原、同时对条件致病性微生物进行鉴别,并与人体共生微生物进行区分,尤其适用于急危重症和疑难感染的诊断。
宏基因组学发展简史
2008年是首例发表的mNGS临床应用报道出现用高通量技术在3例接受实体器官移植的患者样本中检测出沙粒病毒(RNA病毒)的病例。2014年新英格兰杂志刊登了一篇文章:1例患者严重免疫缺陷性疾病的14岁患儿,伴有头部感染症状,4个月的治疗中没有发现任何线索,最后用mNGS在CSF中发现了钩端螺旋体,针对性治疗后康复出院,掀起了mNGS临床应用热潮[1]。到目前为止,mNGS被写入呼吸、感染、重症、检验等多项共识与指南。
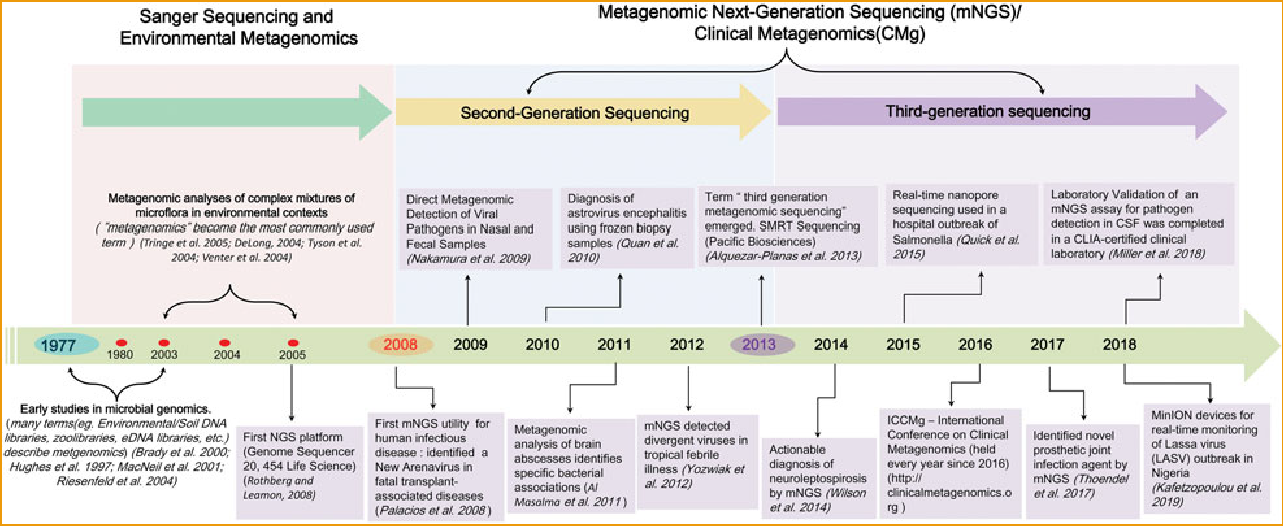
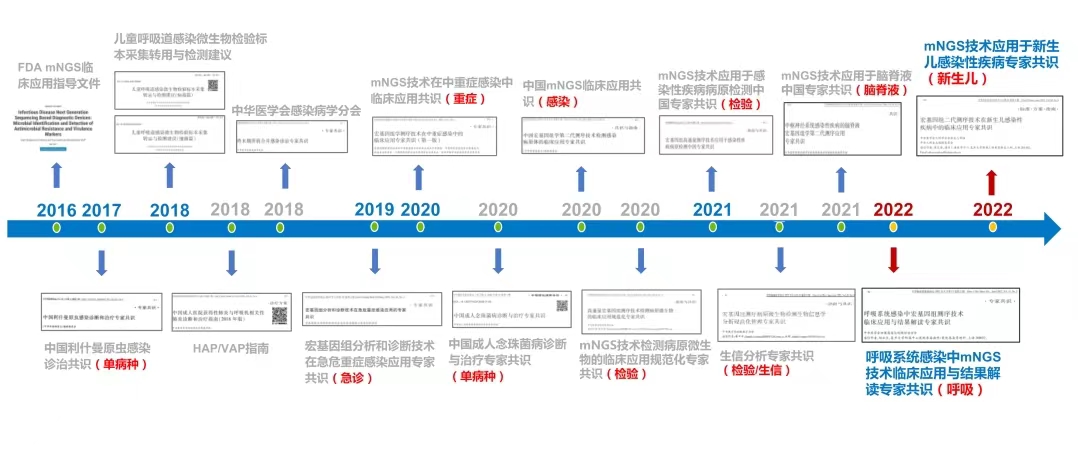
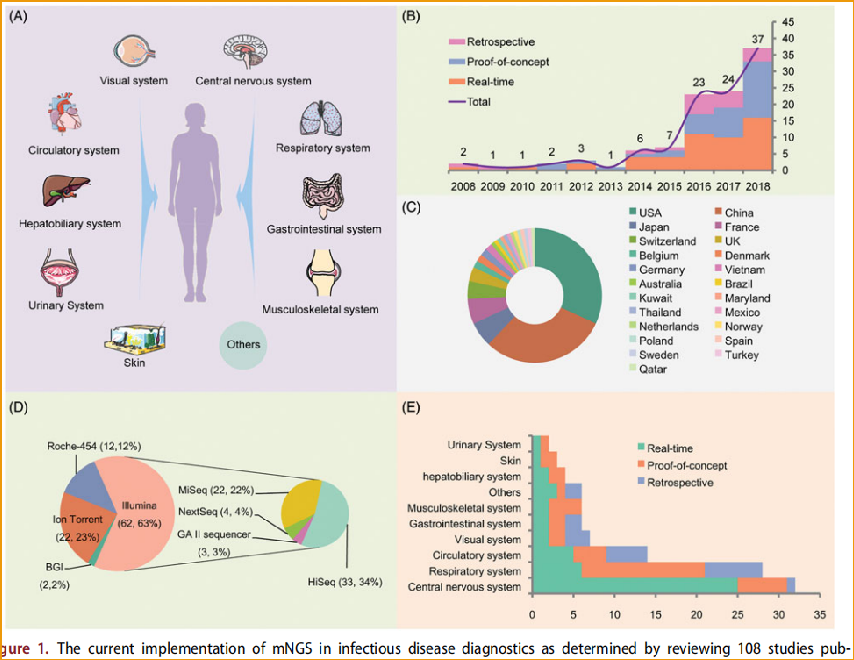
研究分析显示:mNGS临床应用研究逐年迅速增长;其中中国临床应用近占30%;mNGS大部分(62.63%)是采Illumina测序平台;中枢神经系统感染约占mNGS临床应用感染领域的32%,居第一位,其次是呼吸道感染[1]。
2020年2月3日,mNGS在新冠病毒COVID-19的临床应用再起高潮。据悉,复旦大学 张永振 团队在Nature杂志发表文章,该研究对取自一名41岁的男性患者的200μL肺泡灌洗(BALF)提取总RNA进行了深度宏转录组测序,获得完整的病毒基因组(29,903个核苷酸),经比对分析该病毒与一组蝙蝠SARS样冠状病毒最相似,核苷酸相似性高达89.1%。

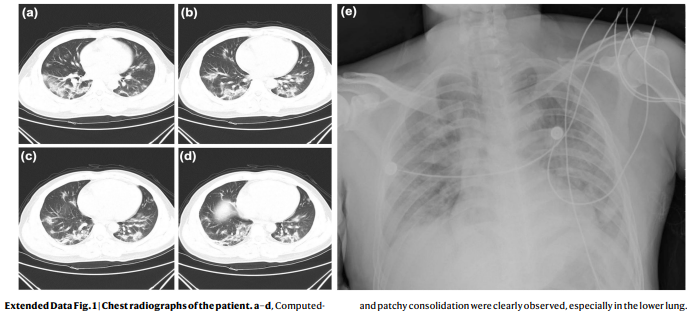
mNGS应用于新冠病毒基因组鉴定只用了5天!
mNGS检测前注意事项
一、DNA与RNA测序的选择
1. DNA与RNA测序流程差异
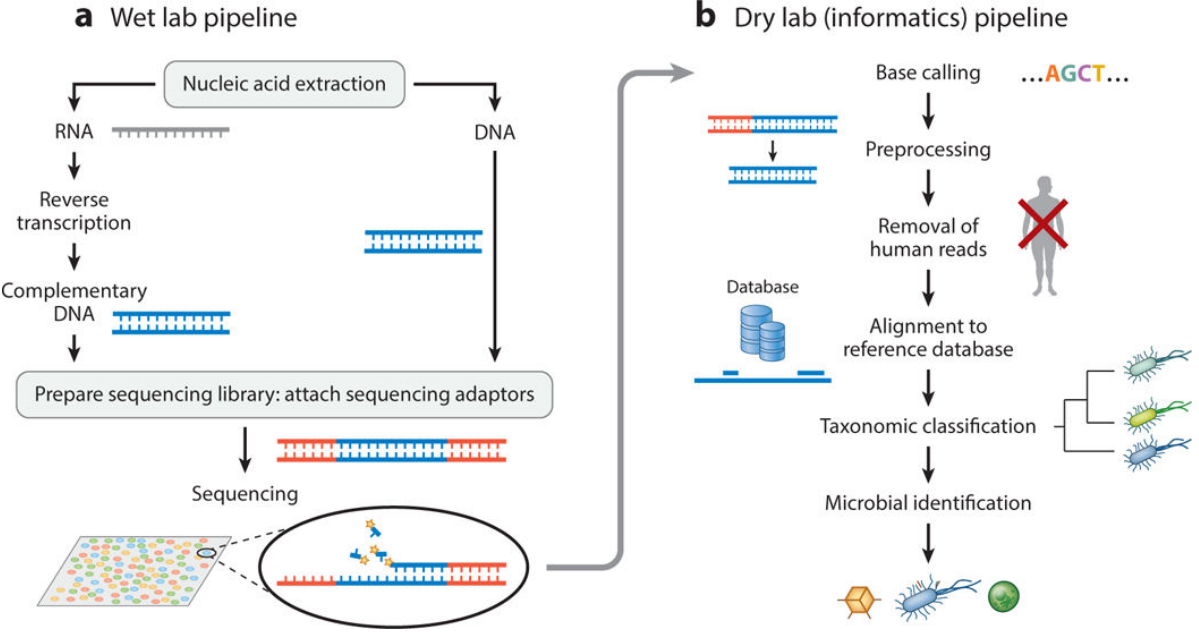
病原微生物高通量检测过程主要包括实验操作 (湿实验) 和生信分析 (干实验) 两个部分。湿实验从收到标本开始,针对不同的样本类型进行特异处理,提取核酸进行文库构建,然后上机测序; 干实验包括下机数据的分析,去人源宿主序列,比对病原微生物数据库,进行种属鉴定,最后解读报告。
2. 临床常见的DNA和RNA病毒

总结:
(1)若怀疑细菌、真菌、DNA病毒、寄生虫、不典型病原体感染且需进行二代测序检测时,建议采用DNA测序;
(2)若怀疑RNA病毒感染时,则建议采用RNA测序[2]。
(3)当怀疑病毒感染,尤其对呼吸道、脑脊液 (cerebrospinal fluid, CSF) 及血液标本,或临床表现复杂,无特定怀疑方向时,需要同时对样本中的DNA和RNA进行测序。
二、感染类型的样本选择
1. mNGS常用临床标本的相关说明[3]

样本的选择一般情况是“哪里感染取哪里”为最宜。但当患者存在感染表现但病情危重或不能耐受有创操作时,可考虑采集患者的血液标本送检(专家共识)。
2. 样本类型采集规范

从正常无菌部位采集mNGS检测标本,应严格无菌操作,避免污染;从有菌定植或污染部位采集的标本,应采取必要措施,尽量减少污染;用于宏基因组RNA测序的标本,应添加核酸稳定剂。mNGS标本的运送须防污染、防震荡、冷链快速运送;标本如不能及时检测,应保存于低于-70 ℃ 冰箱或液氮(血液标本应分离血浆后保存)[3]。
预告:在下篇中,我们将会接着深入了解mNGS临床检测后的注意事项,内容重要且充实,敬请期待!
参考文献
[1]Han Dongsheng; Li Ziyang; Li Rui; Tan Ping, et al. mNGS in clinical microbiology laboratories: on the road to maturity. Critical Reviews in Microbiology, 2019.45(5-6): 668-685.
[2]张文宏. 中国宏基因组学第二代测序技术检测感染病原体的临床应用专家共识. 中华传染病杂志, 2020.38(11):6 81.
[3]王辉等. 宏基因组高通量测序技术应用于感染性疾病病原检测中国专家共识. 中华检验医学杂志, 2021. 44(2): 107-120.